-
 David, da Berlinguer a Gaza i 15 candidati miglior documentario
David, da Berlinguer a Gaza i 15 candidati miglior documentario
-
15enne accoltellato: al vaglio telecamere e testimoni

-
 Le scorte di gas Ue in calo sotto al 55%, in Italia al 62,7%
Le scorte di gas Ue in calo sotto al 55%, in Italia al 62,7%
-
Borsa: l'Europa pesante, bene petrolio e dollaro, giù l'euro

-
 Gruppo Otb conferma Horsting e Snoeren alla guida di Viktor
Gruppo Otb conferma Horsting e Snoeren alla guida di Viktor
-
Anziano in bici travolto e ucciso da camion nel Milanese

-
 Simonelli 'basta personalismi, unità in Serie A e con Figc'
Simonelli 'basta personalismi, unità in Serie A e con Figc'
-
Enasarco, accordo per più impegno per l'economia reale

-
 AC/DC, il 20 luglio a Imola l'unica data italiana
AC/DC, il 20 luglio a Imola l'unica data italiana
-
Processo immediato per l'amico di Ramy, in aula il 18 aprile

-
 Figc: Gravina, mi candido per continuare a unire e cambiare
Figc: Gravina, mi candido per continuare a unire e cambiare
-
Jago, idee? Poco tempo per realizzarle tutte, seleziono

-
 Norvegia da record, elettrico 96% delle auto vendute a gennaio
Norvegia da record, elettrico 96% delle auto vendute a gennaio
-
Pasolini America, da tutto il mondo per studiare il maestro

-
 Fondi 8xmille, a processo il fratello di Becciu e altri otto
Fondi 8xmille, a processo il fratello di Becciu e altri otto
-
Mostra del Cinema di Venezia, da oggi aperte le iscrizioni

-
 Tajani, non discusso ritorno ad immunità, ma non sono contrario
Tajani, non discusso ritorno ad immunità, ma non sono contrario
-
Schlein, il modello Albania è un disastro, ora è chiaro

-
 Abu Mazen, in Cisgiordania in corso una pulizia etnica
Abu Mazen, in Cisgiordania in corso una pulizia etnica
-
Morto il fondatore della milizia ferito in esplosione Mosca

-
 Macron, 'l'Ue sui dazi dovrà farsi rispettare e reagire'
Macron, 'l'Ue sui dazi dovrà farsi rispettare e reagire'
-
Mosca, il voto in Ucraina necessario per accordi di pace

-
 Genovesi trionfa al box office, A Complete Unknown secondo
Genovesi trionfa al box office, A Complete Unknown secondo
-
Lufthansa, a breve l'integrazione con Ita sarà un successo

-
 Calcio: al via assemblea elettiva Figc, tra ospiti Ceferin
Calcio: al via assemblea elettiva Figc, tra ospiti Ceferin
-
Mef, al via le candidature per la Global Money Week

-
 Raid antisemita a Milano, sfregiati murales Bruck-Segre
Raid antisemita a Milano, sfregiati murales Bruck-Segre
-
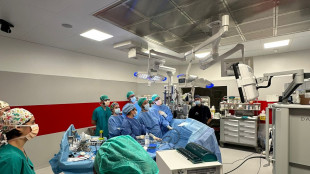
Primo intervento a Meyer con robot chirurgico ultima generazione
-
 Vittima torture di Almasri presenta denuncia contro il Governo
Vittima torture di Almasri presenta denuncia contro il Governo
-
Gallo, 'transizione sostenibile non si può affrontare da soli'

-
 Ricerca: dal Mur oltre 32,1 milioni per le università lombarde
Ricerca: dal Mur oltre 32,1 milioni per le università lombarde
-
OpenAI lancia Deep Research, l'IA per ricerche approfondite

-
 Il Papa, nulla vale quanto la vita di un bambino
Il Papa, nulla vale quanto la vita di un bambino
-
Francesca Ragazzi, il sogno di Vogue Italia in un libro

-
 L'inflazione risale a gennaio all'1,5%
L'inflazione risale a gennaio all'1,5%
-
Almaviva e Fs per la mobilità digitale, nasce Sagitta

-
 Wsj, Cina proporrà a Usa riavvio accordo commerciale 2020
Wsj, Cina proporrà a Usa riavvio accordo commerciale 2020
-
Sci: mondiali al via con parallelo a squadre,fatto team italiano

-
 Sport: patrocinio Vaticano a Run Rome The Marathon per Giubileo
Sport: patrocinio Vaticano a Run Rome The Marathon per Giubileo
-
Milano-Cortina: Bach a Roma, giornata in Vaticano per il n.1 Cio

-
 Scholz, pronti a rispondere ai dazi con i dazi
Scholz, pronti a rispondere ai dazi con i dazi
-
Cremlino, 'per l'Ucraina contatti in via di pianificazione'

-
 Kallas, 'in una guerra dei dazi con gli Usa chi ride è la Cina'
Kallas, 'in una guerra dei dazi con gli Usa chi ride è la Cina'
-
Lady Gaga, nella notte dei Grammy esce il singolo Abracadabra

-
 Altman (OpenAI), non farò causa a DeepSeek
Altman (OpenAI), non farò causa a DeepSeek
-
Borsa: l'Europa paga dazio a Trump, a picco auto e chip

-
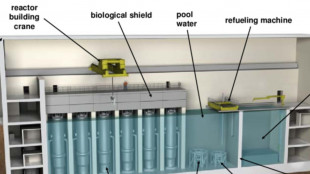 Pichetto, valuteremo interventi in bolletta per il nucleare
Pichetto, valuteremo interventi in bolletta per il nucleare
-
Nel paniere Istat shorts e cono gelato, esce tampone Covid

-
 NBA: Doncic saluta Dallas, "Avrei voluto portarvi un titolo"
NBA: Doncic saluta Dallas, "Avrei voluto portarvi un titolo"
-
Olly, "mi merito il festival, ho fatto tutta la gavetta"

Telethon chiede all'Ue l'autorizzazione a nuova terapia genica
Indicata per la rara sindrome di Wiskott-Aldrich
La Fondazione Telethon ha presentato all'Agenzia europea del farmaco (Ema) la richiesta di autorizzazione all'immissione in commercio per una terapia genica per il trattamento di pazienti con la sindrome di Wiskott-Aldrich, una malattia genetica rara del sistema immunitario. "Un anno fa - ha dichiarato il direttore generale della Fondazione, Ilaria Villa - avevamo annunciato la nostra intenzione di portare all'approvazione la terapia genica per questa rara e grave malattia. Questa nuova tappa conferma sia la promessa fatta alla comunità dei pazienti e ai donatori di rendere le terapie per malattie rare e ultra-rare accessibili e sostenibili, sia l'impegno della Fondazione ad assumere un ruolo sussidiario rispetto agli operatori industriali, ogni qual volta questa sia la condizione necessaria a garantire l'accessibilità della cura". La sindrome di Wiskott-Aldrich è una rara immunodeficienza di origine genetica. Attualmente il solo trattamento potenzialmente risolutivo è il trapianto di cellule staminali del sangue, che tuttavia è realizzabile solo in presenza di un donatore adeguato e non è esente da rischi. La terapia genica ('etuvetidigene autotemcel') fornisce una versione corretta del gene difettoso, grazie a un vettore virale che lo inserisce nelle cellule staminali del sangue prelevate dal paziente. Una volta reinfuse, le cellule corrette sono in grado di ripristinare un sistema immunitario funzionante. La terapia è stata messa a punto dall'Istituto San Raffaele-Telethon per la terapia genica (SR-Tiget) di Milano. A oggi sono complessivamente 30 i pazienti che hanno ricevuto il trattamento. I risultati indicano che la terapia genica è in grado di ripristinare la funzione del sistema immunitario, con una diminuzione delle infezioni, un aumento delle piastrine e un miglioramento delle manifestazioni tipiche come eczema, petecchie ed emorragie. Nei prossimi mesi la richiesta di autorizzazione sarà sottoposta anche alle autorità sanitarie degli Stati Uniti.
E.Hall--AT
